شناساگرهای تشخیصی در رویدادهای قلبی عروقی
شناساگرهای تشخیصی در رویدادهای قلبی عروقی
پیش گفتار : قلب (Heart) بافتی ماهیچه ای (مخطط) دارد و عضو اصلی بدن برای رسانیدن خون و نیازهای تغذیه ای به همه بافتها و سلول های بدن و نیز برگردان Co3H2 و سایر مواد مضر به ارگانهای دفعی است.خود عضله قلب نیز نیاز به اکسیژن و مواد مغذی دارد که این مواد از طریق سرخرگ ها یا (عروق) تاجی Coronary artery به بافت قلب می رسند.
مهمترین از این سرخرگها کرونر سمت چپ است که از آئورت در ناحیه اتصال بطن چپ به آئورت سرچشمه می گیرد و بدو شاخه اصلی تقسیم می شود.
(LMCA) کرونر چپ اصلی یک شاخه به سمت قلب چپ (بطن و دهلیزها می دهد و یک شاخه بنام Circumflex که دور قلب را می پوشاند و تغذیه می کند و یک شاخه Anterior descending که قسمت جلوئی قلب چپ را تغذیه می نماید.
سرخرگ کرونر راست (RCA) عمدتاً بطن و دهلیز راست و گره های SAnode و AVnode که کارشان تنظیم ضربان و ریتم قلب است را خون رسانی می کنند.
و تعداد زیادی سرخرگهای جانبی collateral arteries که در حالت معمول کم فعالند ، ولی در شرایط بحرانی و نارسائی باز شده ئ خون را به بافت قلب میرسانند.
آناتومی قلب و پوشش رگ ها
عکس شماره 1
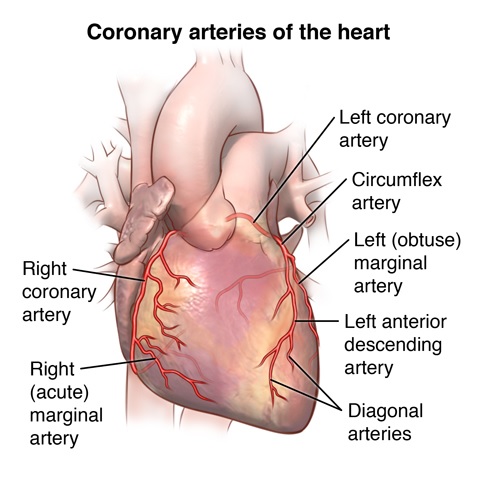
این عکس شاخه های کرونر چپ و ادامه آنها تا آپکس و نیز سرخرگ کرنر راست (RCA) که بطن و دهلیز راست و گره های SAnode و AVnode که کارشان تنظیم ضربان و ریتم قلب است خون رسانی میکنند نشان می دهد.
متابولیزم ریز مغزی ها در تمام سلول ها از مسیر اکسیداسیون احیاء است به جز در گلبولهای قرمز که اکسیژن را حمل می کنند سوخت (کاتابولیسم) به نوعی بدون نیاز به اکسیژن از مسیر متابولیکی دیگری انجام می شود.
در سوخت و ساز هوازی (aerobic) اکسیژن بعنوان آخرین گیرنده الکترون عمل می نمایید و در نتیجه (ATP) که برای فعالیت های آنابولیک و متابولیک لازم است تولید میکند زمانی که سطح اکسیژن خون در عروق سرخرگی پایین باشد عملاً ادامه حیات سلولی با اشکال روبرو می شود. از طرفی عدم برگشت خون سیاهرگی به دهلیز راست که حاوی گازهای بی مصرف و مواد زائد است و پمپ نشدن آن به ریه ها برای اکسیژن گیری مجدداً قلب را با اشکال روبرو می کند و نارسایی قلبی روی میدهد که به آن Ischemic heart disease گفته می شود. .
سلامت و باز بودن عروق کرونر همان قدر اهمیت دارند که حیات و سلامت انسان به نحوی که در برخی بیماریهای حاد میوکارد که سکته ایجاد می شود (Acute Coronary syndrome) که منجر به acute myocardial infarction می شود گاهی قلب به ناگهان از پا می افتد و اصطلاحاً (Arrest) می کند و چنانچه به سرعت عملیات جبرانی و reperfusion صورت نگیرد مرگ ناگهانی می تواند اتفاق بیفتد.
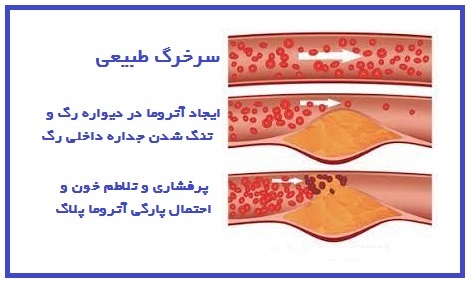
در طول حیات و بخصوص با زندگی کمتر فعال فیزیکی و استفاده از غذاهای پرچرب و نمک سود به مرور در دیواره عروق پلاک های کوچکی شروع به ایجاد شدن می کنند و گاهی این پلاک های آترومائی آنقدر بزرگ می شوند که قطر داخلی رگ (Lumen) را تنگ می کنند. در این جا با پرفشاری خون و تلاطم جریان (turbolance) این پلاک ها پاره می شوند که ممکن است سبب پاره شدن رگ (Dissection) گردد وعمل خون رسانی به بخشی از قلب مختل شود. زمانی که این پلاک ها تحت تأثیر Oxidative Stress و یا پدیده التهابی (Inflammation) قرار می گیرند با پاره شدن پلاک ها مجموعه ای از سلول های التهابی و پلاکت به محل فراخوانده می شوند که این ها نیز با فعال کردن سیستم انعقادی سبب ایجاد لخته و نهایتا ترومبوس رگی می شود و می تواند با تجمع این لخته و بزرگ تر شدن آن راه رگ مسدود و سکته اتفاق بیفتد. اگرچه در گذشته که زندگی فعال تر بود سن سکته قلبی معمولا بالای 50 و یا 60 سال بود امروزه با نوع تغذیه نامناسب (چربیهای ترانس) و بیماریهای زمینه ای مانند دیابت کنترل نشده و سایر عوامل کاردیومیوپاتی، سن سکته گاها به 30 سال یا کمتر رسیده است.
عکس شماره 2
در طول زمان برای مدیریت و شناخت بیماریهای قلبی و در طب مدرن از عوامل مختلف استفاده شده است به نحوی که از سال 1954 دهه 50 و 60 میلادی با استفاده از شناسائی یک بیومارگرهایی مانند Aspartate amino transferase (AST. SGOT) اولین گام ها را برای شناسائی بیماریهای عروق کرونرقلب از طریق شناساگرهای بیولوژیکی برداشته شد .
بیومارگرها: مواد پروتئینی هستند زمانی که قلب و سلول های آن )میوسیت ها( آزرده می شوند، از درون سلول ها آزاد می شوند و طی 1تا5 ساعت سطح پلاسمائی آنها آنقدر می تواند باشد که بوسیله متدهای مختلف آزمایشگاهی قابل شناسائی می شوند.
همانگونه که ذکر شد در سال 55-1954 SGOT اولین مارگر مورد استفاده در این زمینه بود.
بعدها در سالهای 70-1965 LDH- Lactate dehydrogenase و بالا و پایین شدن LDH2 و LDH1 تا حدودی به شناخت بیماری عروق کرونر نزدیک تر شدند. به نحوی که دو ایزوآنزیم LDH1 و LDH2 از بایومارگرهای مهم قلبی به حساب می آمدند.
در سالهای دهه 80-1970 میلادی کراتین کینازتام و بعدتر ایزوآنزیم CK-MB بعنوان یک استاندارد طلائی در تشخیص بیماریهای عروق کرونر مطرح شد و هنوز هم در حافظه تاریخی پزشکان و آزمایشگاهیان CKMB ماندگار است و در برخی مراکز استفاده می شود.
در سالهای دهه 80 میلادی میوگلوبین که پروتئینی آهن دار است و به سرعت بعد از آزردگی میوسیت ها آزاد می شود و همزمان با CKMB به قله (Peak) می رسد ، بعنوان یک بیومارگر مهم مطرح بود. سایر مارگرها مانند هموسیستین (HomoCysteine) که شاید قبل از میوگلوبین آزاد میشود و به سرعت در پلاسما قابل شناسائی است نیز استفاده می شد.
البته در تمام موارد همراهی شناختی این بیومارگرها و علائم قلبی عروقی و ECG (الکتروکاردیوگرام) در تشخیص ACSکمک های زیادی را انجام می دادند، ولی باید توجه داشت اگرچه مارگرهای ذکر شد از حساسیت بالائی برخوردار بودند ولی می توانند از سایر سلول های بدن و بافتهای آزرده آزاد شوند و بنابراین ویژگی خاص برای سلول های میوکارد یا نداشتند و یا ویژگی پائینی دارند.
در سالها دهه 90 میلادی و بخصوص از سال 2000 و تا کنون تعداد بی شماری از شناساگر های قلبی شناخته شده اند که برخی از آنها بعلت سختی سنجش کمی به مرور حذف شده اند .
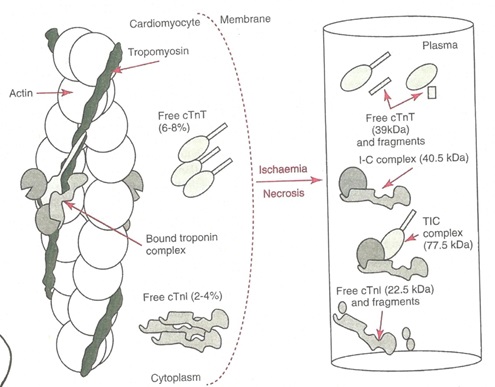
تروپونین ها : پروتئین های هستند که بعضی مانند تروپونین آی ویژگی بالایی برای سلول های قلب دارد. تروپنین تی که اگر چه هنوز هم ویژگی آن برای سلولهای میوکارد بالااست ولی در سایر بافتهای ماهیچه ای مخطط نیز وجود دارند .تروپونین سی که اگر چه در سلول های قلبی هستند ولی ویژگی خاص برای سلولهای قلب ندارند
Troponin I 23.8 KDa
Troponin I 36 KDa
Troponin I 18.4 KDa
این مجموعه پروتینی با کمک کلسیم (Ca) عمل انقباض و انبساط میوفیبریل های میوکارد (آکیتن و میوزین ) را بعهده دارند
عکس منحنی آزاد شدن تروپونین و CKMB و سایر مارکر ها بعد از حوادث قلبی
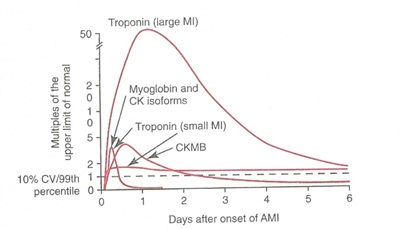
روپونین آی اگر چه از همان ابتدای آسیب به میوکارد آزاد می شود ولی در سکته های کوچک مقادیر آن کم است و با سرعت از پلاسما پاک می شوند .ایزوآنزیم cr-mbنیز از ابتدا آزاد می شوند و مدت زمان بیشتری در پلاسمامی ماند ولی ویژگی آن برای قلب زیاد نیست .در سکته های وسیع میزان CTNIبالا می رود و تا چندین روز در پلاسما قابل تشخیص است .
نیمه عمر تروپونین تقریباً 2 ساعت است به نحوی که مقادیر ناچیز Troponin هم اگر در سرم شناسائی شود می تواند نشانه های سکته های خیلی کوچک (Micro Infarction) باشد.
باز هم توجه شما را به این نکته جلب می کنیم که انیز cTnI خاص ماهیچه های قلب است ولی در آسیب های جدی (trauma) به ماهیچه های اسکلتی مقادیری از (cTnT) در سرم قابل شناسائی هستند. بعنوان مثال در مواردی drmatomyositis ، polymyositis و بیماری های کلیوی end stage و نارسائی کلیوی (renal failure) در سرم دیده می شود. به همین خاطر امروزه در بیشتر آزمایشگاها و نیز مراکز کاردیولوژی (و جراحی قلب) از تروپونین I (cTnI) بعنوان بیومارگر اختصاصی استفاده می شود. اگرچه هنوز هم بعضی از مراکز جهانی از تروپونین T نیز استفاده می نمایند.
باید در نظر داشت که هنوز یک واحد که نشان دهنده 99th percentile از مقادیر CTn باشد بوسیله شرکت های عمده تولید کننده کیت های تروپونین معرفی نشده است. شرکت های معتبر تولید کننده با متدهای فوق حساس (highsensitivity) . cTnI مانند Abott و عدد منفی برای تروپویین را بین یک صدم تا چهار صدم میکروگرم در لیتر را تا 99thpercentile منفی می کنند. و عدد مثبت را تا micro/L 8. در سیستم بیومریو مقادیر کمتر از 19نانوگرم در لیتر را منفی و مقادیر 19 تا 100نانو گرم در لیتر را حد وسط و مقادیر بیشتر از 100 نانوگرم در لیتر را مثبت تلقی می کنند. در تمامی مراحل آزمایش بمنظور حفظ ارزش بالینی تست تروپونین باید به عوامل تداخل کننده با روند آزمایش آشنا بود وحتی المقدور آنها را حذف نمود.
عواملی که بصورت کاذب سبب پایین نشان دادن مقدار تروپونین ها می شوند وجود بیوتین یا ویتامین B7 ، افزایش بیلی روبین و هموگلوبین در سرم، آتوآنتی بادی های تولیدشده بر علیه تروپونین آی ، ای دی تی آ و احتمالاً هپارین سبب False negative و یا پایین نشان دادن مقادیر Troponin I میشوند.
برخی مواد مانند لخته فیبرین ، اتصال ملکولهای بزرگ به تروپونین، می توانند مقادیر Troponin I را بصورت کاذب بالاتر از حد حقیقی آن نشان دهند.در افراد بالای 65 سال و بیماران مبتلا به بیماری های کلیوی همیشه مقادیر تروپونینT بیشتر از دامنه منفی ممکن است دیده شود که در این موارد تکرار تست بعد از 6 ساعت پیشنهاد میگردد.
بهترین گزینه در سیستم های تروپونین آسی بسته (Closed troponin Assay) سرم است اگرچه برخی استفاده از خون سرانگشت را مستقیماً روی کاست هائی که با توان micro capillary خون را بداخل کاست می کشند و واکنش را انجام می دهند بعنوان یک POCT آزمایش در بالین بیمار به کار می برند.
و یا شرکت و روش hs –cTnT Assays - Elecsys- Roche 99thpercentile برای منفی را 0.001 و مقادیر مثبت 99th Percentile را 8 mg/L قرار داده است. و مقادیر بین این دو را بعنوان Gray-Zone و یا Borderline تلقی نموده است شرکت بیومریو که از یکی از معتبرترین سازندگان کیت های (Closed) است مقادیر
منفی Negative <19 ng/Liter
حد وسط Borderline 19-100ng/Liter
مثبت Positive >100ng/Liter
تلقی نموده است.
در واقع (cTnT) و (cTnI) بوسیله ژنوم میوسیت ها کدگذاری میشوند ولی (cTnC) را می توان در بافت های آزرده و مزمن کلیوی Chronic renal disease و همچنین در سلول های
Gastro intestinal Tract یافت.
در واقع چون cTnI و cTnT ویژگی بالائی برای ماهیچه قلب دارند این دو را بیشتر بعنوان شناساگرهای (Biomarker) قلب می شناسند.
سطح تروپونین T و I معمولا سه تا 4 ساعت بعد از حمله قلبی (سکته AMI) بالا می آید در صورتیکه می توان با متدهای (assay) های نسل پنجم که حساسیت بالائی داشته باشند، آنها را اندازه گیری نمود. در صورتیکه با متدها (assay) های نسل چهارم سنجیده شوند معمولا 4تا9 ساعت بعد از AMI قابل شناسائی هستند 12تا14 ساعت بعد از سکته قلبی به بالاترین حد (Peak) می رسند و 14تا10 روز هم بعد از حمله قلبی هم چنان قابل شناسائی هستند.
- خلاصه شده : تست های لازم بعد از ایجاد و یا احتمال سکته قلبی که از 4 تا 6 ساعت بعد از حادثه باید انجام شود Troponin I 1) چون طی 14-12 ساعت به Peak می رسد. معمولاً هر 6 ساعت یک بار انجام می شود هر چه میزان CInI بالاتر باشد، نشان از شدت بیشتر سکته قلبی است و پیش آگهی خوبی ندارد. اگر بعد از 24 ساعت سطح CTnI به مرور پائین بیاید، نشان دهنده جبران خون رسانی reperfusion می باشد.
این آیزو آنزیم CK نیز چون خیلی زود شروع به آزاد شدن CK-MB از میوسیت های آزرده می کند- مارگر خوبی تلقی می شود.
3- High Sensitivity CRP
که یک مدیاتور التهابی است که در زمان التهاب در کبد به میزان قابل توجهی تولید می شود و وارد خون می شود. این CRP هم می تواند خاصیت آتروژنیک داشته باشد و به بدتر شدن قضیه AtheroSclerosis کمک کند و هم افزایش پیش از حد آن پیش آگهی خوبی را نوید نمی دهد.
باید توجه داشت که در هر موردی که تهاجم (Invasioin) به بافت قلب و عروق آن پیش می آید مانند پیوند عروق کرونر Coronary artery bypass Graft یا CABG در جریان Angio Plasty و قرار دادن Stent و حتی در موارد اسپاسم عروق قلب می تواند در سرم بعد از 6 ساعت قابل مشاهده باشد.
دکتر برات عبودی
آزمایشگاه بیمارستان شهریار




